Mamíferos Podem Ter Poderes Regenerativos Ocultos, Revela Estudo
Durante séculos, os livros de biologia traçaram uma linha dura entre humanos e animais como as salamandras: os mamíferos curam com cicatrizes; os anfíbios regeneram membros. Mas uma nova pesquisa da Texas A&M University sugere que essa distinção pode ser menos sobre impossibilidade biológica e mais sobre uma mudança oculta que permanece intacta na cura humana.
Um estudo publicado em* Nature Communications * demonstra que os ratos podem regenerar ossos, articulações, ligamentos e tendões após a amputação. A chave não foi introduzir novas células estaminais, mas sim redirecionar a resposta celular existente do corpo para longe de cicatrizes e para a regeneração.
Embora os tecidos regenerados não fossem anatomicamente perfeitos, os resultados desafiam a suposição de longa data de que os mamíferos perderam a capacidade de regenerar estruturas complexas. Este avanço pode abrir caminho para novos tratamentos que reduzam as cicatrizes e melhorem a reparação tecidual, aproximando potencialmente a medicina regenerativa da realidade clínica.
Religar a resposta de cura
Quando um mamífero sofre uma lesão grave, como uma amputação, a prioridade imediata do organismo é a sobrevivência. As células de fibroblastos correm para o local da ferida para selá-lo rapidamente, formando tecido cicatricial. Este processo, conhecido como fibrose, protege o corpo de infecções e perda de sangue, mas efetivamente interrompe a possibilidade de regenerar estruturas perdidas.
Em contraste, animais regenerativos como as salamandras formam um * * blastema— * – uma massa temporária de células que atua como um suporte para o crescimento de novos tecidos.
O Dr. Ken Muneoka, professor do Texas A&M College of Veterinary Medicine and Biomedical Sciences, passou sua carreira investigando por que essa diferença existe. Sua equipe descobriu que os fibroblastos de mamíferos não são inerentemente incapazes de regeneração. Em vez disso, eles estão presos em uma “via cicatriz” por padrão.
“É como se essas células pudessem se mover em duas direções diferentes”, explicou Muneoka. “Eles poderiam fazer uma cicatriz ou fazer um blastema. A nossa investigação centrou-se no redirecionamento do comportamento dos fibroblastos já presentes no local da lesão.”
Uma Estratégia De Tratamento Em Duas Etapas
Os pesquisadores desenvolveram um tratamento sequencial em duas etapas usando dois fatores de crescimento bem conhecidos para induzir o corpo a regenerar o tecido.
-
** Primeiro Passo: Evitar Cicatrizes
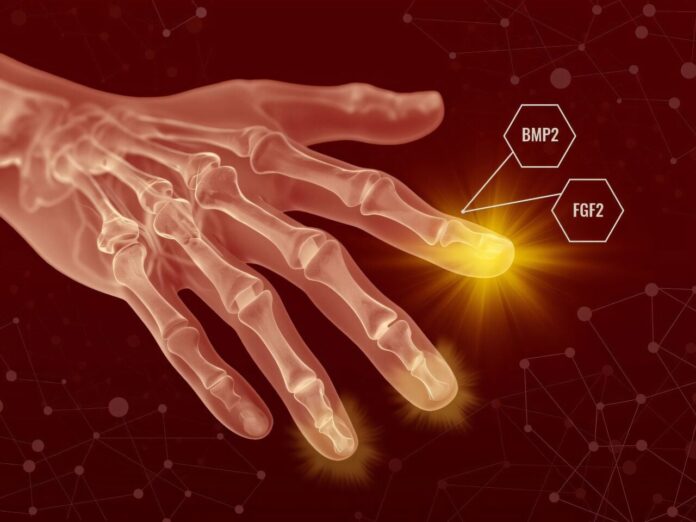
Após o fechamento da ferida inicial, a equipe aplicou * * Fator de crescimento de fibroblastos 2 (FGF2). Esta etapa permitiu que o corpo terminasse seu processo de cicatrização padrão, mas depois sinalizou que os fibroblastos parassem de formar tecido cicatricial e, em vez disso, começassem a se organizar em uma estrutura semelhante ao blastema. -
** Passo Dois: Construir Novo Tecido
Vários dias depois, os pesquisadores aplicaram proteína Morfogenética óssea 2 (BMP2)**. Este segundo sinal instruiu a massa celular recém-formada a se diferenciar em tecidos específicos, incluindo osso, tendão e ligamento.
“Este é realmente um processo de duas etapas”, disse Muneoka. “Você primeiro afasta as células das cicatrizes e, em seguida, fornece os sinais que lhes dizem o que construir.”
Desafiando o paradigma das células estaminais
Uma das implicações mais significativas deste estudo é o seu desafio às atuais estratégias de medicina regenerativa, que muitas vezes dependem da colheita e transplante de células estaminais.
O Dr. Larry Suva, co-autor do estudo, observou que a capacidade de regeneração não estava ausente nos mamíferos—era apenas obscurecida pelo mecanismo de cura padrão do corpo.
“As células que pensávamos não serem programáveis, na verdade, são”, disse Suva. “Você não precisa realmente pegar células-tronco e colocá-las de volta. Eles já estão lá — você só precisa aprender como fazê-los se comportar da maneira que você quiser.”
O estudo também revelou um fenômeno chamado * * re-Especificação posicional**, onde as células foram guiadas para formar estruturas fora de sua posição anatômica original. Isto sugere que as células dos mamíferos mantêm um modelo flexível de desenvolvimento, que pode ser reactivado nas condições adequadas.
Rebrota imperfeita mas funcional
Os membros regenerados nos ratinhos não eram réplicas perfeitas da anatomia original. As estruturas careciam da simetria precisa e dos detalhes finos do crescimento natural. No entanto, continham todos os componentes essenciais removidos durante a amputação: ossos, estruturas articulares, tendões e ligamentos.
“Nós regeneramos o que você esperaria ver nesse nível de lesão”, disse Muneoka. “As estruturas estão lá — mas não numa forma perfeita.”
Esta imperfeição evidencia a complexidade da regeneração. Não se trata de um simples interruptor de ligar/desligar, mas de um processo multifacetado que envolve múltiplas vias biológicas. Embora os resultados ainda não estejam prontos para aplicação humana, eles fornecem uma prova crítica de conceito: a falha regenerativa de mamíferos pode ser resgatada.
Caminhos para a aplicação clínica
Embora o crescimento de membros inteiros em humanos continue a ser um objetivo distante, as aplicações imediatas desta pesquisa podem ser mais modestas, mas igualmente impactantes. A abordagem em duas etapas poderia ser adaptada para reduzir as cicatrizes e melhorar a qualidade da reparação tecidual em cirurgias e lesões normais.
O caminho clínico a seguir pode ser mais suave do que o previsto, porque ambos os fatores de crescimento já são familiares à comunidade médica:
* * * BMP2 * * já está aprovado pela FDA para certos procedimentos ortopédicos.
* * * O FGF2 * * está actualmente a ser submetido a vários ensaios clínicos.
Como esses agentes não são totalmente novos, os obstáculos regulatórios podem ser menores, permitindo que os pesquisadores testem como pequenas mudanças no processo de cicatrização podem produzir benefícios significativos no tratamento de feridas e no reparo tecidual.
Conclusão
Este estudo marca uma mudança crucial na nossa compreensão da biologia dos mamíferos. Ao provar que o mecanismo de regeneração existe dentro de nós—dormente, mas acessível -, os investigadores abriram novas portas para a inovação médica. O futuro da medicina regenerativa pode não estar na importação de células estranhas, mas na aprendizagem da linguagem Reparadora do próprio corpo.