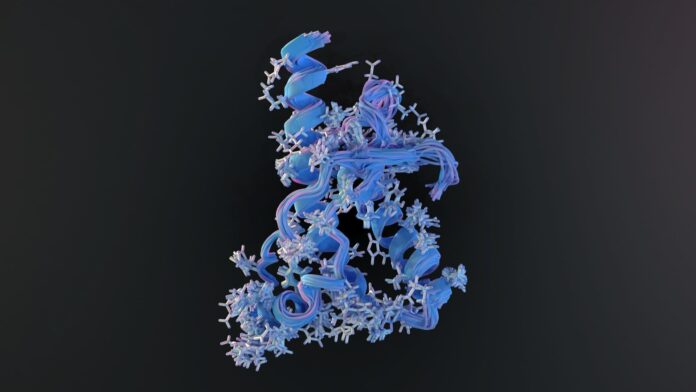
Le 9 avril 1982, une publication scientifique dans la revue Science a fondamentalement modifié notre compréhension des maladies infectieuses. Le Dr Stanley Prusiner, alors à l’Université de Californie à San Francisco, a présenté la preuve qu’une maladie pouvait être causée non pas par un virus ou une bactérie, mais par une protéine infectieuse. Cette découverte a remis en question les fondements mêmes de la biologie moléculaire et a fait découvrir au monde le prion.
Le mystère du « virus lent »
Pendant des décennies, les scientifiques ont été déconcertés par un groupe de troubles dégénératifs du cerveau partageant des similitudes frappantes. Ceux-ci comprenaient :
– Tremblante : Une maladie mortelle affectant les moutons et les chèvres.
– Kuru : Un désordre dévastateur observé dans la tribu Fore de Papouasie-Nouvelle-Guinée.
– Maladie de Creutzfeldt-Jakob (MCJ) : Un trouble implacable du cerveau humain.
Au microscope, les tissus cérébraux des victimes de ces maladies semblaient remarquablement similaires : criblés de minuscules trous qui donnaient à l’organe une apparence « spongiforme » ou semblable à une éponge.
Parce que ces maladies progressaient lentement et ne présentaient pas les caractéristiques typiques d’une infection, telles que la fièvre ou l’activation du système immunitaire, les scientifiques les ont initialement classées comme des « virus lents ». Il restait cependant un énorme vide logique : si ces maladies étaient causées par des virus, elles devraient contenir des acides nucléiques (ADN ou ARN). De plus, le fait que certains cas semblaient être familiaux suggérait une composante génétique qui ne correspondait pas à la transmission virale standard.
Remettre en question le « dogme central »
La percée a eu lieu lorsque Prusiner a orienté ses recherches de la MCJ vers la tremblante, suite aux découvertes du radiobiologiste Tikvah Alper. Alper avait démontré que la tremblante pouvait toujours être transmise même après que les tissus aient été traités à la lumière ultraviolette, un processus qui détruit l’ADN.
Cette observation suggérait que l’agent infectieux était totalement dépourvu de matériel génétique. Grâce à une expérimentation rigoureuse utilisant des hamsters (qui ont accéléré la progression de la maladie aux fins d’étude), Prusiner a isolé le coupable. Il a prouvé que l’agent infectieux était une protéine, qu’il a baptisée “prion”.
C’était une affirmation révolutionnaire car elle contredisait le ** « dogme central » de la biologie moléculaire **. Le dogme central postule que l’information circule de l’ADN à l’ARN puis aux protéines ; l’idée qu’une protéine seule puisse agir comme un agent infectieux – essentiellement « codant » pour sa propre réplication en forçant les protéines saines à mal se replier – semblait impossible aux yeux de l’establishment scientifique de l’époque.
Comment fonctionnent les prions : une réaction en chaîne d’un mauvais pliage
Le scepticisme entourant le travail de Prusiner a finalement cédé la place à des preuves accablantes. Au cours des 15 années suivantes, les chercheurs ont cartographié le mécanisme de la maladie à prions :
- Changement conformationnel : Les prions sont des protéines qui se sont repliées dans une forme anormale et pathologique.
- Infection basée sur un modèle : Lorsqu’un prion rencontre une version saine de la même protéine, il agit comme un modèle, forçant la protéine saine à « se retourner » pour prendre la forme malade.
- Résistance : Contrairement à la plupart des protéines, les prions sont incroyablement résistants et résistent à la dégradation par les processus naturels de dégradation du corps.
Si les prions sont à l’origine de l’infection, la science moderne a également clarifié le lien avec la génétique : certaines mutations de l’ADN peuvent prédisposer les individus à créer ces protéines mal repliées, expliquant pourquoi certains cas semblent héréditaires.
La découverte du prion a prouvé que les règles les plus fondamentales de la vie pouvaient être contournées par une seule molécule mal repliée.
Conclusion
L’identification du prion par Stanley Prusiner a comblé le fossé entre les maladies infectieuses et la pathologie génétique, ce qui lui a valu le prix Nobel en 1997. Ses travaux ont transformé la neurologie et fourni un nouveau cadre pour comprendre comment les protéines peuvent agir comme agents de vie et de mort.