Durante siglos, los libros de texto de biología han trazado una línea dura entre los humanos y los animales como las salamandras: los mamíferos sanan con cicatrices; los anfibios vuelven a crecer las extremidades. Pero una nueva investigación de la Universidad Texas A&M sugiere que esta distinción puede tener menos que ver con la imposibilidad biológica y más con un interruptor oculto que permanece inalterado en la curación humana.
Un estudio publicado en * Nature Communications demuestra que los ratones pueden regenerar huesos, articulaciones, ligamentos y tendones después de la amputación. La clave no fue introducir nuevas células madre, sino más bien redirigir la respuesta celular existente del cuerpo * lejos de las cicatrices y hacia la regeneración.
Si bien los tejidos regenerados no eran anatómicamente perfectos, los hallazgos desafían la suposición arraigada de que los mamíferos han perdido la capacidad de regenerar estructuras complejas. Este avance podría allanar el camino para nuevos tratamientos que reduzcan las cicatrices y mejoren la reparación de tejidos, acercando potencialmente la medicina regenerativa a la realidad clínica.
Recableando la Respuesta Curativa
Cuando un mamífero sufre una lesión grave, como una amputación, la prioridad inmediata del organismo es la supervivencia. Las células de fibroblastos se apresuran al sitio de la herida para sellarla rápidamente, formando tejido cicatricial. Este proceso, conocido como fibrosis, protege al cuerpo de infecciones y pérdida de sangre, pero cierra efectivamente la posibilidad de que vuelvan a crecer las estructuras perdidas.
Por el contrario, los animales regenerativos como las salamandras forman un * * blastema**, una masa temporal de células que actúa como andamio para el crecimiento de tejido nuevo.
El Dr. Ken Muneoka, profesor de la Facultad de Medicina Veterinaria y Ciencias Biomédicas de Texas A&M, dedicó su carrera a investigar por qué existe esta diferencia. Su equipo descubrió que los fibroblastos de mamíferos no son inherentemente incapaces de regenerarse. En cambio, están atrapados en una “vía de cicatrización” de forma predeterminada.
“Es como si estas células pudieran moverse en dos direcciones diferentes”, explicó Muneoka. “Podrían hacer una cicatriz o hacer un blastema. Nuestra investigación se centró en redirigir el comportamiento de los fibroblastos ya presentes en el sitio de la lesión.”
Una Estrategia de Tratamiento en Dos Pasos
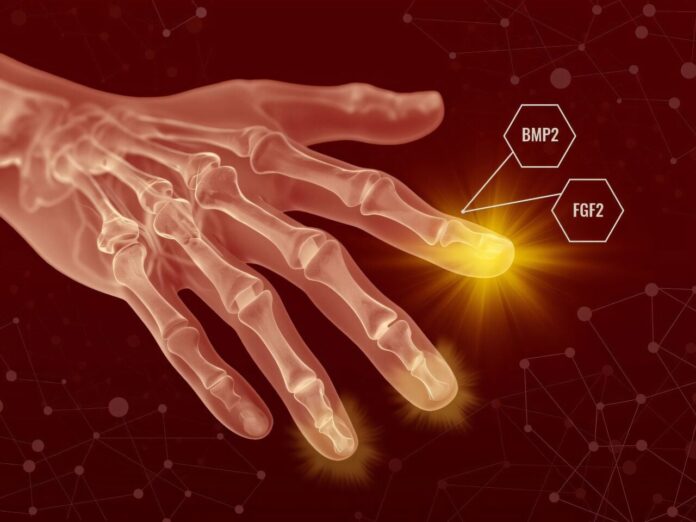
Los investigadores desarrollaron un tratamiento secuencial de dos pasos utilizando dos factores de crecimiento bien conocidos para engañar al cuerpo para que regenere el tejido.
-
** Paso Uno: Prevenir Cicatrices
Después de que se cerró la herida inicial, el equipo aplicó * * Factor de crecimiento de Fibroblastos 2 (FGF2). Este paso permitió que el cuerpo terminara su proceso de curación estándar, pero luego indicó a los fibroblastos que dejaran de formar tejido cicatricial y, en cambio, comenzaran a organizarse en una estructura similar a un blastema. -
** Paso Dos: Construir Tejido Nuevo
Varios días después, los investigadores aplicaron * * Proteína Morfogenética Ósea 2 (BMP2). Esta segunda señal instruyó a la masa celular recién formada a diferenciarse en tejidos específicos, incluidos huesos, tendones y ligamentos.
“Este es realmente un proceso de dos pasos”, dijo Muneoka. “Primero, aleja las células de la cicatrización y luego les proporciona las señales que les dicen qué construir .”
Desafiando el Paradigma de las Células Madre
Una de las implicaciones más significativas de este estudio es su desafío a las estrategias actuales de medicina regenerativa, que a menudo dependen de la recolección y el trasplante de células madre.
El Dr. Larry Suva, coautor del estudio, señaló que la capacidad de regeneración no estaba ausente en los mamíferos, simplemente estaba oscurecida por el mecanismo de curación predeterminado del cuerpo.
“Las células que pensamos que no eran programables, de hecho, lo son”, dijo Suva. “En realidad, no es necesario obtener células madre y volver a colocarlas. Ya están allí, solo necesita aprender a hacer que se comporten de la manera que desea.”
El estudio también reveló un fenómeno llamado * * reespecificación posicional**, donde las células fueron guiadas para formar estructuras fuera de su posición anatómica original. Esto sugiere que las células de mamíferos conservan un plan flexible para el desarrollo, que puede reactivarse en las condiciones adecuadas.
Rebrote Imperfecto pero Funcional
Las extremidades regeneradas en los ratones no eran réplicas perfectas de la anatomía original. Las estructuras carecían de la simetría precisa y los finos detalles del crecimiento natural. Sin embargo, contenían todos los componentes esenciales extraídos durante la amputación: huesos, estructuras articulares, tendones y ligamentos.
“Regeneramos lo que esperarías ver a ese nivel de lesiones”, dijo Muneoka . “Las estructuras están ahí, pero no en una forma perfecta.”
Esta imperfección resalta la complejidad de la regeneración. No es un simple interruptor de encendido/apagado, sino un proceso multifacético que involucra múltiples vías biológicas. Si bien los resultados aún no están listos para su aplicación en humanos, proporcionan una prueba crítica de concepto: * * se puede rescatar la falla regenerativa de los mamíferos.**
Vías de Aplicación Clínica
Si bien el recrecimiento de extremidades enteras en humanos sigue siendo un objetivo distante, las aplicaciones inmediatas de esta investigación pueden ser más modestas pero igualmente impactantes. El enfoque de dos pasos podría adaptarse para reducir las cicatrices y mejorar la calidad de la reparación de tejidos en cirugías y lesiones estándar.
El camino clínico hacia adelante puede ser más fluido de lo previsto porque ambos factores de crecimiento ya son familiares para la comunidad médica:
* * * BMP2 * * ya está aprobado por la FDA para ciertos procedimientos ortopédicos.
* * * FGF2 * * se encuentra actualmente en varios ensayos clínicos.
Debido a que estos agentes no son completamente nuevos, los obstáculos regulatorios pueden ser menores, lo que permite a los investigadores probar cómo pequeños cambios en el proceso de curación pueden producir beneficios significativos en el cuidado de heridas y la reparación de tejidos.
Conclusión
Este estudio marca un cambio fundamental en nuestra comprensión de la biología de los mamíferos. Al demostrar que la maquinaria para la regeneración existe dentro de nosotros, inactiva pero accesible, los investigadores han abierto nuevas puertas para la innovación médica. El futuro de la medicina regenerativa puede no estar en importar células extrañas, sino en aprender a hablar el lenguaje de reparación del propio cuerpo.