Seit Jahrhunderten ziehen Biologielehrbücher eine harte Grenze zwischen Menschen und Tieren wie Salamandern: Säugetiere heilen mit Narben; Amphibien wachsen Gliedmaßen nach. Neue Forschungsergebnisse der Texas A & M University legen jedoch nahe, dass es bei dieser Unterscheidung weniger um biologische Unmöglichkeit als vielmehr um einen versteckten Schalter geht, der bei der menschlichen Heilung nicht umgedreht wird.
Eine in * Nature Communications * veröffentlichte Studie zeigt, dass Mäuse Knochen, Gelenke, Bänder und Sehnen nach Amputation regenerieren können. Der Schlüssel war nicht die Einführung neuer Stammzellen, sondern die ** Umleitung der vorhandenen zellulären Reaktion des Körpers ** weg von der Narbenbildung und hin zur Regeneration.
Während die regenerierten Gewebe anatomisch nicht perfekt waren, stellen die Ergebnisse die lang gehegte Annahme in Frage, dass Säugetiere die Fähigkeit verloren haben, komplexe Strukturen nachwachsen zu lassen. Dieser Durchbruch könnte den Weg für neue Behandlungen ebnen, die die Narbenbildung reduzieren und die Gewebereparatur verbessern und die regenerative Medizin möglicherweise der klinischen Realität näher bringen.
Neuverkabelung der Heilungsreaktion
Wenn ein Säugetier eine schwere Verletzung erleidet, wie zum Beispiel eine Amputation, ist die unmittelbare Priorität des Körpers das Überleben. Fibroblastenzellen eilen zur Wundstelle, um sie schnell zu versiegeln und Narbengewebe zu bilden. Dieser Prozess, der als Fibrose bekannt ist, schützt den Körper vor Infektionen und Blutverlust, schließt jedoch effektiv die Möglichkeit des Nachwachsens verlorener Strukturen aus.
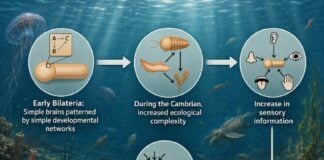
Im Gegensatz dazu bilden regenerative Tiere wie Salamander ein ** Blastem ** — eine temporäre Zellmasse, die als Gerüst für neues Gewebewachstum dient.
Dr. Ken Muneoka, Professor am Texas A & M College für Veterinärmedizin und biomedizinische Wissenschaften, hat seine Karriere damit verbracht, zu untersuchen, warum dieser Unterschied besteht. Sein Team entdeckte, dass Säugetierfibroblasten von Natur aus nicht regenerationsunfähig sind. Stattdessen sind sie standardmäßig in einem “Narbenweg” gefangen.
“Es ist, als ob sich diese Zellen in zwei verschiedene Richtungen bewegen könnten”, erklärte Muneoka. “Sie könnten entweder eine Narbe machen oder ein Blastem machen. Unsere Forschung konzentrierte sich auf die Umlenkung des Verhaltens von Fibroblasten, die bereits an der Verletzungsstelle vorhanden sind.”
Eine zweistufige Behandlungsstrategie
Die Forscher entwickelten eine sequentielle zweistufige Behandlung mit zwei bekannten Wachstumsfaktoren, um den Körper dazu zu bringen, Gewebe zu regenerieren.
-
** Erster Schritt: Narbenbildung verhindern
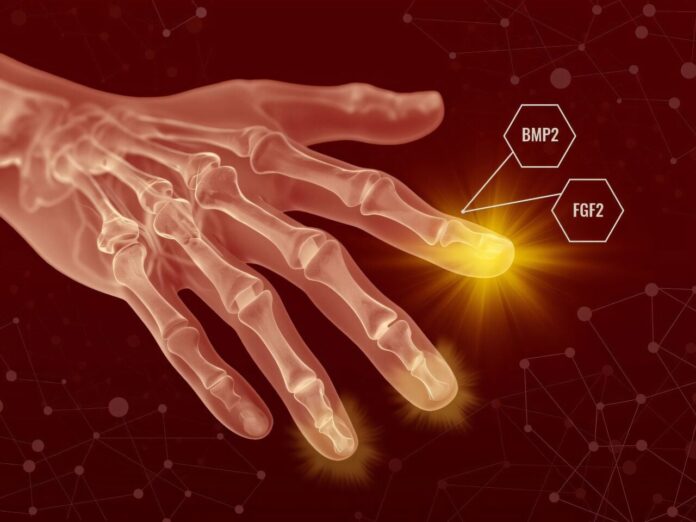
Nachdem die erste Wunde geschlossen war, applizierte das Team ** Fibroblastenwachstumsfaktor 2 (FGF2) . Dieser Schritt ermöglichte es dem Körper, seinen normalen Heilungsprozess zu beenden, signalisierte dann aber den Fibroblasten, die Bildung von Narbengewebe einzustellen und stattdessen mit der Organisation zu einer blastemartigen Struktur zu beginnen. -
** Schritt zwei: Neues Gewebe aufbauen
Einige Tage später applizierten die Forscher ** knochenmorphogenetisches Protein 2 (BMP2) . Dieses zweite Signal wies die neu gebildete Zellmasse an, sich in spezifische Gewebe, einschließlich Knochen, Sehnen und Bänder, zu differenzieren.
“Das ist wirklich ein zweistufiger Prozess”, sagte Muneoka. “Sie verschieben zuerst die Zellen weg von der Narbenbildung, und dann liefern Sie die Signale, die ihnen sagen, was sie bauen sollen.”
Das Stammzell-Paradigma in Frage stellen
Eine der wichtigsten Implikationen dieser Studie ist ihre Herausforderung für aktuelle Strategien der regenerativen Medizin, die häufig auf der Ernte und Transplantation von Stammzellen beruhen.
Dr. Larry Suva, ein Mitautor der Studie, stellte fest, dass die Regenerationsfähigkeit bei Säugetieren nicht fehlte – sie wurde lediglich durch den Standardheilungsmechanismus des Körpers verdeckt.
“Die Zellen, die wir für unprogrammierbar hielten, sind es tatsächlich”, sagte Suva. “Sie müssen keine Stammzellen bekommen und sie wieder einsetzen. Sie sind bereits da – Sie müssen nur lernen, wie Sie sie dazu bringen, sich so zu verhalten, wie Sie es möchten.”
Die Studie enthüllte auch ein Phänomen, das als Positionsrespezifikation bezeichnet wird, bei dem Zellen dazu geführt wurden, Strukturen außerhalb ihrer ursprünglichen anatomischen Position zu bilden. Dies deutet darauf hin, dass Säugetierzellen einen flexiblen Bauplan für die Entwicklung behalten, der unter den richtigen Bedingungen reaktiviert werden kann.
Unvollkommenes, aber funktionelles Nachwachsen
Die regenerierten Gliedmaßen der Mäuse waren keine perfekten Nachbildungen der ursprünglichen Anatomie. Den Strukturen fehlte die genaue Symmetrie und die feinen Details des natürlichen Wachstums. Sie enthielten jedoch alle wesentlichen Bestandteile, die bei der Amputation entfernt wurden: Knochen, Gelenkstrukturen, Sehnen und Bänder.
“Wir haben das regeneriert, was man bei dieser Verletzungsstufe erwarten würde”, sagte Muneoka. “Die Strukturen sind da – nur nicht in perfekter Form.”
Diese Unvollkommenheit unterstreicht die Komplexität der Regeneration. Es ist kein einfacher Ein- / Ausschalter, sondern ein facettenreicher Prozess, an dem mehrere biologische Wege beteiligt sind. Obwohl die Ergebnisse noch nicht für die Anwendung beim Menschen bereit sind, liefern sie einen kritischen Proof of Concept: ** Regenerationsversagen bei Säugetieren kann gerettet werden.**
Wege zur klinischen Anwendung
Während das Nachwachsen ganzer Gliedmaßen beim Menschen ein fernes Ziel bleibt, können die unmittelbaren Anwendungen dieser Forschung bescheidener, aber ebenso wirkungsvoll sein. Der zweistufige Ansatz könnte angepasst werden, um die Narbenbildung zu reduzieren und die Qualität der Gewebereparatur bei Standardoperationen und Verletzungen zu verbessern.
Der klinische Weg könnte reibungsloser verlaufen als erwartet, da beide Wachstumsfaktoren der medizinischen Gemeinschaft bereits bekannt sind:
* ** BMP2 ** ist bereits von der FDA für bestimmte orthopädische Eingriffe zugelassen.
* ** FGF2 ** befindet sich derzeit in mehreren klinischen Studien.
Da diese Wirkstoffe nicht ganz neu sind, können die regulatorischen Hürden niedriger sein, sodass Forscher testen können, wie geringfügige Verschiebungen im Heilungsprozess erhebliche Vorteile bei der Wundversorgung und Gewebereparatur bringen können.
Schlussfolgerung
Diese Studie markiert einen entscheidenden Wandel in unserem Verständnis der Säugetierbiologie. Durch den Nachweis, dass die Regenerationsmaschinerie in uns existiert — ruhend, aber zugänglich — haben Forscher neue Türen für medizinische Innovationen geöffnet. Die Zukunft der regenerativen Medizin liegt möglicherweise nicht darin, fremde Zellen zu importieren, sondern zu lernen, die körpereigene Sprache der Reparatur zu sprechen.