Po staletí byly v biologických učebnicích jasně definovány hranice mezi lidmi a zvířaty, jako jsou mloci: savci se hojí s jizvami a obojživelníci znovu dorůstají končetiny. Nový výzkum z University of Texas A&M (Texas A&M University) však naznačuje, že tento rozdíl není ani tak o biologické nemožnosti, jako spíše o skrytém “přepínači”, který v procesu hojení zůstává u člověka neaktivní.
Studie publikovaná v časopise * Nature Communications * ukazuje, že myši jsou schopny regenerovat kosti, klouby, vazy a šlachy po amputaci. Klíčem k úspěchu nebylo zavedení nových kmenových buněk, ale** přesměrování stávající buněčné reakce těla * * od tvorby jizvy k regeneraci.
Ačkoli regenerované tkáně nebyly anatomicky dokonalé, tyto objevy zpochybňují dlouhodobé přesvědčení, že savci ztratili schopnost růst složitých struktur. Tento průlom by mohl připravit cestu k novým léčebným postupům, které snižují tvorbu jizev a zlepšují obnovu tkání, což by potenciálně přiblížilo regenerativní medicínu ke klinickému použití.
Přeprogramování procesu hojení
Když je savec vážně zraněn, jako je amputace, je prioritou těla přežití. Fibroblastové buňky spěchají na místo rány, aby ji rychle uzavřely a vytvořily jizvu. Tento proces, známý jako fibróza, chrání tělo před infekcí a ztrátou krve, ale účinně blokuje možnost růstu ztracených struktur.
Naproti tomu regenerativní zvířata, jako jsou mloci, vytvářejí blastem — dočasný shluk buněk, který funguje jako rám pro růst nové tkáně.
Dr. Ken Munoka, profesor na University of Texas A&M College of veterinary medicine and Biomedical Sciences, věnoval svou kariéru výzkumu příčin tohoto rozdílu. Jeho tým zjistil, že savčí fibroblasty nejsou zpočátku schopny regenerace. Místo toho se ve výchozím nastavení “zaseknou” na cestě k vytvoření jizvy.
“Zdá se, že tyto buňky se mohou pohybovat dvěma různými směry,” vysvětlil Munoco. — Mohou buď vytvořit jizvu, nebo vytvořit blastém. Naše studie se zaměřila na přesměrování chování fibroblastů již přítomných v místě poškození.”
Dvoustupňová léčebná strategie
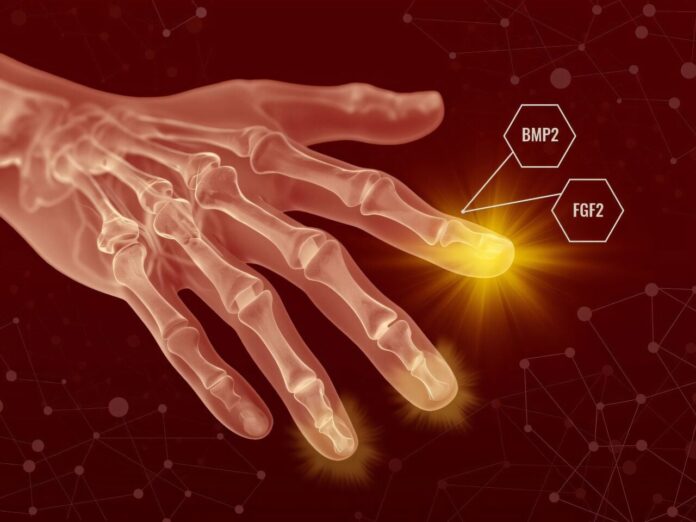
Výzkumníci vyvinuli konzistentní dvoustupňovou terapii pomocí dvou dobře známých růstových faktorů, aby “oklamali” tělo a donutili ho regenerovat tkáň.
-
** Fáze první: prevence vzniku jizvy
Po počátečním uzavření rány tým použil * * fibroblastový růstový faktor 2 (FGF2). Tento krok umožnil tělu dokončit standardní proces hojení a poté vyslal signál fibroblastům, aby zastavily tvorbu jizvy a začaly se organizovat do struktury připomínající blastém. -
** Fáze druhá: budování nové látky
O několik dní později vědci aplikovali * * kostní morfogenetický protein 2 (BMP2). Tento druhý signál dal pokyn nově vytvořené buněčné hmotě, aby se diferencovala do konkrétních tkání, včetně kosti, šlach a vazů.
“Je to opravdu dvoustupňový proces,” řekl Munoc. — Nejprve přepnete buňky z režimu zjizvení a poté poskytnete signály, které jim řeknou, co přesně mají postavit.”
Výzva paradigmatu kmenových buněk
Jedním z nejvýznamnějších důsledků této studie je její zpochybňování současných strategií regenerativní medicíny, které se často opírají o plot a transplantaci kmenových buněk.
Dr. Larry Suva, spoluautor studie, poznamenal, že schopnost regenerace u savců nechyběla — byla jednoduše skryta za standardním mechanismem hojení těla.
“Buňky, které jsme považovali za neprogramovatelné, jsou ve skutečnosti poddajné,” řekl Suva. – Není nutné extrahovat kmenové buňky a vracet je zpět. Už jsou uvnitř — stačí se naučit, jak je přimět, aby se chovali, jak potřebujete.”
Studie také identifikovala jev zvaný poziční respecifikace, při kterém byly buňky zaměřeny na tvorbu struktur mimo jejich původní anatomickou polohu. To naznačuje, že savčí buňky si zachovávají flexibilní “výkres” vývoje, který lze reaktivovat za správných podmínek.
Nedokonalý, ale funkční růst
Regenerované končetiny u myší nebyly přesnými kopiemi původní anatomie. Struktury jsou laděny přesnou symetrií a jemnými detaily přirozeného růstu. Obsahovaly však všechny hlavní složky ztracené při amputaci: kosti, kloubní struktury, šlachy a vazy.
“Zregenerovali jsme to, co se dalo očekávat při takové úrovni poškození,” řekl Muno. “Struktury tam jsou, jen ne v dokonalé formě.”
Tato nedokonalost podtrhuje složitost regenerace. Není to jednoduchý přepínač “zapnuto / vypnuto”, ale mnohostranný proces, který zahrnuje mnoho biologických drah. I když výsledky ještě nejsou připraveny k použití u lidí, poskytují kritický důkaz konceptu: selhání regenerace u savců lze odstranit.
Cesty ke klinickému použití
Zatímco růst celých končetin u lidí zůstává vzdáleným cílem, přímé použití těchto studií může být skromnější, ale neméně smysluplné. Dvoufázový přístup lze přizpůsobit ke snížení tvorby jizev a zlepšení kvality opravy tkání při standardních chirurgických zákrocích a úrazech.
Klinická cesta vpřed může být hladší, než se očekávalo, protože oba růstové faktory jsou již známé lékařské komunitě:
* * * BMP2 * * je již schváleno FDA pro určité ortopedické postupy.
* * * FGF2 * * v současné době probíhá několik klinických studií.
Vzhledem k tomu, že tato činidla nejsou zcela nová, regulační bariéry mohou být nižší, což výzkumníkům umožní testovat, jak malé změny v procesu hojení mohou mít významný přínos v péči o rány a obnově tkání.
Závěr
Tato studie představuje zlom v našem chápání biologie savců. Tím, že vědci dokázali, že v nás existují regenerační mechanismy — spící, ale cenově dostupné — otevřely nové dveře lékařským inovacím. Budoucnost regenerativní medicíny nemusí spočívat v zavádění cizích buněk, ale v učení se mluvit vlastním jazykem obnovy našeho těla.